26上高中化学教资面试(试讲逐字稿+试讲真题+答辩+面试模板+结构化等)
- 2026-06-04 14:07:13
资料适合26上教资面试/考编试讲
资料全套包括:试讲示范视频、试讲稿逐字稿、试讲面试真题、答辩、历年高频考题、结构化押题等
【最新整理有高中化学面试题本+简案+试讲稿+配套对应的试讲视频】
(部分示例)
试讲面试历年真题有300多页(必看)
一、考题


二、解析
【教学过程】
(一)导入新课
【教师提问】回忆一下初中学过的知识,什么是氧化反应,什么是还原反应,能不能举出几个具体的实例呢?
【学生回答】氧化反应:碳与氧气、铁与氧气……
还原反应:氢气还原氧化铜、碳还原氧化铜、一氧化碳还原氧化铜……

(二)新课讲授
1.氧化还原反应的特征
【提出问题】能不能举出其他的氧化还原反应?
【学生回答】碳与氧化铜的反应、氢气还原氧化铜……
【提出问题】观察一下所列举的几个化学方程式,除了得失氧之外,从化合价的角度思考什么是氧化还原反应?
【学生回答】得氧元素发生氧化反应,元素化合价升高;失氧元素发生还原反应,元素化合价降低。
【教师引导】由此可知,氧化还原反应的特征就是有元素化合价升降的变化。
【提出问题】铁与硫酸铜的反应是否属于氧化还原反应?是不是只有得失氧的化学反应才是氧化还原反应?
【学生回答】是,铁元素、铜元素的化合价都出现了变化。可知并不是只有得失氧的反应才是氧化还原反应。
2.氧化还原反应的本质
【提出问题】为什么在氧化还原反应中会出现化合价的升降变化?元素化合价的升降与什么有关?
【学生回答】元素化合价的变化与得失电子(电子转移)有关。
【教师引导】那么就从原子结构的角度揭秘在氧化还原反应中,元素的化合价为什么会发生变化。
【提出问题】金属钠在氯气中燃烧生成NaCl,从原子结构示意图的角度思考NaCl是怎样形成的?
【学生思考,教师讲解】从原子结构来看,钠原子的最外电子层上有1个电子,氯原子的最外电子层上有7个电子。当钠与氯气反应时,钠原子失去1个电子,带1个单位正电荷,成为钠离子(Na+);氯原子得到1个电子,带1个单位负电荷,成为氯离子(Cl-)。这样双方最外电子层都达到了8个电子的稳定结构。钠元素的化合价由0价升高到+1价,被氧化;氯元素的化合价由0价降低到-1价,被还原。在这个反应中,发生了电子的得失,金属钠发生了氧化反应,氯气发生了还原反应。(教师讲解并板书,利用双线桥法)。
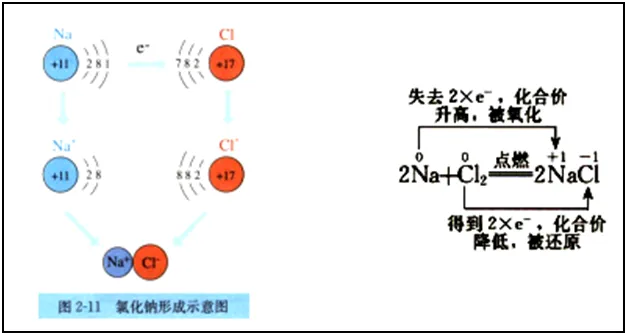
【提出问题】氢气在氯气中燃烧生成HCl,从原子结构示意图的角度思考HCl是怎样形成的?
【学生思考,教师讲解】从原子结构来看,氢原子最外层有1个电子,可获得1个电子而形成2个电子的稳定结构。氯原子的最外电子层上有7个电子,也可获得1个电子而形成8个电子的稳定结构。
这两种元素的原子获取电子难易程度相差不大。在发生反应时,它们都未能把对方的电子夺取过来,而是双方各以最外层的1个电子组成一个共用电子对,这个电子对受到两个原子核的共同吸引,使对方最外电子层都达到稳定结构。在氯化氢分子里,由于氯原子对共用电子对的吸引力比氢原子的稍强一些,所以,共用电子对偏向氯原子而偏离于氢原子。因此,氢元素的化合价从0价升高到+1价,被氧化;氯元素的化合价从0价降低到-1价。在这个反应中,发生了共用电子对的偏移,氢气发生了氧化反应,氯气发生了还原反应。(教师讲解并板书)
【提出问题】根据以上的分析,能不能从电子转移的角度重新定义氧化还原反应?
【学生回答】有电子转移(得失或偏移)的反应,是氧化还原反应。(教师总结并板书)
【提出问题】能不能从电子转移的角度分析铁与硫酸铜的反应?
【学生回答】铁元素失去2个电子,化合价升高,发生氧化反应;铁元素得到2个电子,化合价降低,发生还原反应。(教师板书:利用双线桥法)
(三)巩固提升
【提出问题】有人说置换反应、有单质参加的化合反应和有单质生成的分解反应全部属于氧化还原反应,你认为这个说法正确吗?请说明理由。
提示:正确。因为在这几类反应中,反应前后都有元素化合价发生变化。
(四)小结作业
请学生回答本堂课的收获:氧化还原反应的特征、本质,学到了什么?
布置作业:课下思考,四大反应类型与氧化还原反应有什么关系。
【板书设计】
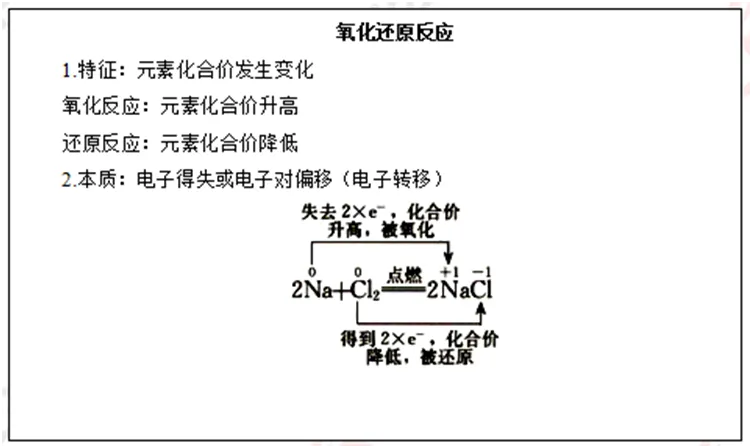
【答辩题目解析】
1.说明四种基本反应类型与氧化还原反应之间的关系?
【参考答案】
置换反应一定是氧化还原反应,复分解反应一定不是氧化还原反应,化合反应及分解反应不一定是氧化还原反应。
2.简单介绍一下本节课的设计思路?
【参考答案】
复习旧识,引导发现→重新定义氧化还原反应→通过对比化学方程式发现氧化还原反应判断的方法→内化知识,总结出氧化还原反应的本质→教师讲解氧化还原反应的表示方法→巩固练习→归纳总结,预留任务。




 精选高频试讲真题示范视频,配套对应的题本内容+简案+试讲逐字稿,让面试学习理解更容易!(面试必看)
精选高频试讲真题示范视频,配套对应的题本内容+简案+试讲逐字稿,让面试学习理解更容易!(面试必看)

高中化学试讲稿有150多篇(部分有题本+简案+逐字稿+答辩)
高中化学《丁达尔效应》逐字稿
谢谢各位评委老师,我今天试讲的篇目是《丁达尔效应》,下面开始我的试讲。
(一)导入新课
上课,同学们好,请坐。在上节课我们学习了分散系,谁能帮助我们回忆一下什么是分散系?好,请你来。他说把一种物质分散在另一种物质中所得到的体系叫做分散系。看来你课下有进行复习,这种学习态度非常好,快请坐。
如何区分溶液、胶体和浊液呢。嗯,同桌,你来。同桌说可以根据分散质粒子的大小进行区分。溶液中溶质粒子通常小于1nm,浊液中的粒子通常大于100nm,胶体粒子大小在1~100nm之间。你概括的十分全面,对上节课的知识掌握的很牢固,请坐。可有些液态胶体也是透明的,用肉眼很难与溶液区分,如何将它们区分开呢?这节课咱们就继续走进化学课堂,学习新课《丁达尔效应》。
(二)新课讲授
同学们请看,老师在烧杯中加入25毫升蒸馏水,将烧杯中的蒸馏水加热至沸腾,向沸水中逐滴加入6滴氯化铁饱和溶液,继续煮沸至溶液呈红褐色,停止加热。这时我们所得到的就是氢氧化铁胶体。
现在请同学们看老师讲台上分别放置的氢氧化铁胶体、硫酸铜溶液和泥水。通过观察。大家可以发现哪些化学信息呢?嗯,你来说,他说硫酸铜溶液属于稳定的分散系,而泥水属于浊液,也就是不稳定的分散系,氢氧化铁胶体介于二者之间,在一定条件下可以稳定存在。
你的知识学的可真扎实。没错,溶液属于稳定分散系,浊液为不稳定的分散系,而胶体属于介稳体系。接下来老师将盛有硫酸铜溶液和氢氧化铁胶体的烧杯置于暗处,分别用激光笔照射烧杯中的液体,请一位同学在与光束垂直的方向进行观察。靠窗的女同学你来代表大家观察一下,你所观察到的实验现象是什么呢?
她发现光束照射氢氧化铁胶体时有光亮的通路,而硫酸铜溶液无光亮的通路。你描述的十分准确,快请回。其实这一条光亮的通路是由于胶体粒子对光线散射而形成的。我们把它叫做丁达尔效应。所以我们就可以利用丁达尔效应来区分胶体与溶液。
我们学会用实验区分胶体和溶液,那如何区分胶体和浊液呢?老师听到同学们说可以通过胶体和浊液的粒子大小来区分,接下来咱们就用实验来证明我们的猜想吧。下面请同学们自己来动手操作一下,将氢氧化铁胶体和泥水分别进行过滤,观察并记录实验现象。我们以化学小组为单位进行实验,老师会进行巡视指导,如果有问题可以举手示意。
看到大家实验都基本完成了,谁来说一说你们的实验现象是什么呢?二组请你们来,他们发现氢氧化铁胶体的分散质能通过滤纸,而泥水的分散质不能通过滤纸。大家的实验现象是否与二组同学一致呢?好看来大家实验都做得很成功。
通过这个实验,我们可以得出怎样的结论呢?嗯,三组你们来。三组说,这就说明了浊液的分散质粒子比胶体的大。你的思维可真活跃,快请坐。因此我们可以通过过滤的方法来去区分浊液和胶体。
通过刚刚的实验,我们能够区分胶体、溶液和浊液,丁达尔效应在日常生活中随处可见,请同学们试着举出例子,同桌之间可以相互交流讨论。开始吧。你们组的想法非常的独特,请你们来,他们说电影院放映室射到银幕上的光柱,还有光线透过树叶的缝隙射入森林都是丁达尔效应。好,前面的同学,你们也想分享,他们说猫眼石也是丁达尔效应。
看来大家在日常生活中都有留心观察。同学们请看这是老师为大家播放的几组关于丁达尔效应的图片,这些美景是我们在生活中很常见,我们可以感受到化学和生活息息相关。
(三)巩固小结
我们这堂课的新知识就学习完成了,请同学们看多媒体这里有溶液、胶体和浊液我们如何进行区分呢。嗯,同学们都说溶液和胶体可以通过丁达尔效应判断,胶体和浊液可以通过实验过滤的方法来进行区分。看来大家对本节课的知识都掌握的很牢固。
不知不觉一堂课就要接近尾声了,谁来说一说你在本堂课有哪些收获呢?老师听到有的同学说,这一节课知道了丁达尔效应的原理,也了解了生活中常见的丁达尔效应,学会了区分溶液、胶体和浊液,看来大家这一堂课都是收获满满。
(四)布置作业
就让我们带着这种收获和感悟,在课后完成课后习题,并且查阅资料,搜集生活中常见的丁达尔效应,下节课我们一起来分享交流。
好,同学们,这节课就上到这里,下课。








考前一周更新鸭题
(年年押,年年中)
资料已打包好
面试各科都有,需要全套可以咨询我们
一站式复习备考

